
유한양행이 자체 개발 항암신약 ‘렉라자’에 대한 미국 식품의약국(FDA) 허가를 받아 연구·개발(R&D) 역량을 입증했다.
21일 제약바이오업계에 따르면 유한양행은 2014년 국내 제약업계에서 최초로 매출 1조 원을 돌파해 선두 기업으로 꼽혔다. 그러나 매출 대부분이 글로벌 제약사에서 도입한 제품 판매 실적으로 구성돼 사실상 ‘수입품 도매상’이라는 꼬리표를 달고 있었다. 하지만 이번 FDA 승인으로 수년간 투자를 아끼지 않았던 R&D 성과가 결실을 맺었다는 평가가 나온다.
FDA는 19일(현지시간) 유한양행이 개발한 비소세포폐암 신약 렉라자와 존슨앤드존슨이노베이티브메디슨(구 얀센)의 이중항체 치료제 ‘리브리반트(성분명 아미반타맙)’ 병용요법을 폐암 1차 치료제로 허가했다.
존슨앤드존슨이노베이티브메디슨은 지난해 말 FDA에 렉라자와 리브리반트 병용요법에 대한 허가를 신청했고, FDA는 올해 2월 21일 이를 우선심사 대상으로 지정했다. FDA 우선심사 대상 목록에 이름을 올린 약제는 6개월 내 심사 결과를 받을 수 있다.
렉라자가 FDA 문턱을 넘으면서 유한양행은 본격적으로 미국을 비롯한 글로벌 항암제 시장 진출에 시동을 건다. FDA가 세계 각국의 의약품 규제기관들이 참고하는 글로벌 표준점으로 여겨진다는 점을 고려하면, 유한양행이 렉라자를 앞세워 글로벌 빅파마 대열에 합류할 가능성도 기대할 수 있다.
국내 개발 항암 신약의 미국 진출은 렉라자가 최초다. 유한양행이 국내 제약사들 가운데 체질개선 성과를 가장 먼저 가시화한 셈이다. 그간 유한양행을 비롯한 국내 기업들은 제네릭 의약품 및 수입 품목에 매출을 의존하는 구조에서 벗어나, 신약과 신기술 개발로 경쟁력을 강화하는 쇄신 작업에 열을 올렸다.
유한양행은 2015년 오스코텍의 미국 자회사 제노스코로부터 15억 원에 신약 후보 물질 레이저티닙을 도입했다. 국내에서 임상 1~2상을 진행하고 2018년 글로벌 빅파마인 존슨앤드존슨이노베이티브메디슨에 한국을 제외한 지역에서의 레이저티닙 개발 및 상업화 권리를 이전하는 12억5500만 달러(1조6724억 원) 규모의 계약을 맺었다. 이후 두 회사는 레이저티닙 개발을 위해 협력했으며, 국내에서는 유한양행이 2021년 1월 식품의약품안전처로부터 31번째 국산 신약으로 허가를 받았다.
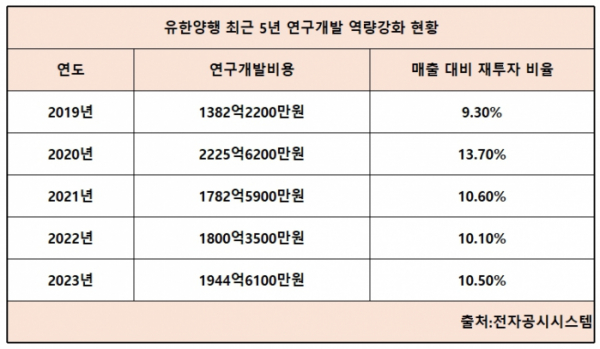
유한양행은 9년여 만에 R&D에 강한 기업으로 체질 개선에 성공했다. 레이저티닙을 도입한 2015년 당시 유한양행은 R&D 투자비로 약 726억 원을 썼다. 매출 대비 투자비율은 6.4%로, 2014년(5.7%)과 비교하면 늘었지만, 10%를 넘지 않는 수준이었다. 2015년 말 기준 특허등록건수는 국내 170건, 해외 378건으로 총 548건이었다.
지난해 기준 유한양행은 매출의 10.5%인 1944억 원을 R&D에 재투자했다. 매출 대비 R&D 투자 비율은 꾸준히 상승했으며, 2020년 2225억 원(13.7%)을 써 처음으로 10%대에 진입했다. 이후 2021년 1782억 원(10.6%), 2022년 1800억 원(10.1%) 등 4년 연속으로 10%를 초과하고 있다. 지난해 말 기준 특허등록건수는 국내 209건, 해외 710건으로 총 919건에 달했다.
유망한 파이프라인도 다수 보유했다. 미국에서 임상 2a상을 완료한 위마비증 치료제 YH12852, 미국 임상 3상 단계인 퇴행성 디스크 치료제 YH14618 등이 제2의 렉라자가 될 것으로 기대 중이다. 국내에서는 지아이이노베이션에서 알레르기 치료제 YH35324를 도입하고, 에이비엘바이오와 항암제 YH32367를 공동연구하는 등 적극적인 오픈이노베이션 전략도 구사하고 있다.
개방적인 연구협업과 장기적인 투자가 유한양행의 성공 요인으로 지목된다. 한 국내 제약·바이오 업계 전문가는 “글로벌 빅파마와 비교해 국내 기업은 자금력과 인력 측면에서 아직까지 한계가 있어, 이를 극복하기 위한 기업 간 오픈이노베이션뿐 아니라 민·관, 산·학 등의 다각도 협업이 이뤄져야 한다”라며 “R&D 투자비의 절대적인 규모도 중요하지만, 장기적으로 투입할 수 있는지가 관건이라서 기업의 의지와 투자자들의 신뢰가 필요하다”라고 말했다.

!["이미 결제된 선수입니다"…본격 막 올린 스토브리그, '변수'는 없을까? [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2098040.jpg)
![먹을 사람 없고 귀찮아서…"김장, 안 하고 사 먹어요" [데이터클립]](https://img.etoday.co.kr/crop/140/88/2098061.jpg)

![[단독] "AI에 진심" 정태영 부회장, '유니버스' 중동 세일즈 나섰다](https://img.etoday.co.kr/crop/140/88/1970536.jpg)







![[내일 날씨] 전국 대부분 아침 기온 5도 내외…얼음 어는 곳도](https://img.etoday.co.kr/crop/85/60/2098154.jpg)









![[정치대학] 美 대선, 막판까지 초박빙…당선자별 韓 영향은?](https://img.etoday.co.kr/crop/300/170/2098110.jpg)
!['한국의 장 담그기 문화' 유네스코 무형문화유산 등재 유력 [포토]](https://img.etoday.co.kr/crop/300/190/2098066.jpg)