국내 연구진이 수학적 모델을 이용해 세포질 혼잡을 유발하는 비만과 치매, 노화가 어떻게 불안정한 수면을 유발하는지를 밝히고 해결책을 제시했다.
한국과학기술원(KAIST)은 수리과학과 김재경 교수 연구팀이 수학적 모델을 이용해 세포 내 분자 이동을 방해하는 세포질 혼잡이 불안정한 일주기 리듬과 수면 사이클을 유발함을 예측하고, 미국 플로리다 주립대학 이주곤 교수 연구팀과 실험을 통해 검증하는 데 성공했다고 9일 밝혔다.
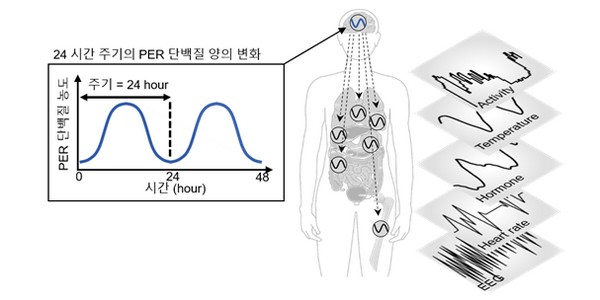
우리 뇌 속에 있는 생체시계는 밤 9시경이 되면 뇌 속에서 멜라토닌 호르몬의 분비를 유발해 일정 시간에 잠을 잘 수 있도록 하는 등 운동 능력이나 학습 능력에 이르기까지 거의 모든 생리 작용에 관여한다.
2017년 노벨생리의학상을 받은 마이클 영, 제프리 홀, 마이클 로스바쉬 교수는 핵심 생체시계(PER) 단백질이 매일 일정한 시간에 세포핵 안으로 들어가 PER 유전자의 전사를 일정 시간에 스스로 억제하는 음성피드백 루프를 통해 24시간 주기의 리듬을 만드는 것이 생체시계의 핵심 원리임을 밝혔다. 하지만 다양한 물질이 존재하는 복잡한 세포 내 환경에서 어떻게 수천 개의 PER 단백질이 핵 안으로 일정한 시간에 들어갈 수 있는지는 오랫동안 생체시계 분야의 난제로 남아있었다.
김 교수 연구팀은 난제 해결을 위해 세포 내 분자의 움직임을 묘사하는 시공간적 확률론적 모형을 자체 개발했다. 이를 이용해 분석한 결과 PER 단백질이 세포핵 주변에서 충분히 응축돼야만 동시에 인산화돼 핵 안으로 함께 들어간다는 사실을 알아냈다. 또 PER 단백질의 핵 주변 응축을 방해하는 지방 액포와 같은 물질들이 세포 내에 과도하게 많아져 세포질이 혼잡해지면 인산화 스위치가 작동하지 않아 불안정한 일주기 리듬과 수면 사이클이 유발된다는 사실도 확인했다.
김 교수팀의 수리 모델 예측은 미국 플로리다 주립대학 이주곤 교수팀과 협업을 통해 실험으로 검증하는 한편 한 발짝 더 나가 비만ㆍ치매ㆍ노화가 세포질 혼잡을 일으킴으로써 수면 사이클의 불안정을 가져오는 핵심 요인임을 규명하는 데도 성공했다.
김 교수는 “비만과 치매, 그리고 노화가 불안정한 수면을 유발하는 원인을 수학과 생명과학의 융합 연구를 통해 밝힌 연구”라며 ”이번 성과를 통해 수면 질환의 새로운 치료법이 개발되기를 기대한다“고 말했다.
한편 KAIST 수리과학과 김대욱 박사과정이 공동 제1 저자로 참여한 이번 연구 결과는 국제 학술지 ‘미국국립과학원회보(PNAS)’ 10월 26일 자 온라인판에 실렸다.


!["이미 결제된 선수입니다"…본격 막 올린 스토브리그, '변수'는 없을까? [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2098040.jpg)
![먹을 사람 없고 귀찮아서…"김장, 안 하고 사 먹어요" [데이터클립]](https://img.etoday.co.kr/crop/140/88/2098061.jpg)

![[단독] "AI에 진심" 정태영 부회장, '유니버스' 중동 세일즈 나섰다](https://img.etoday.co.kr/crop/140/88/1970536.jpg)








![[내일 날씨] 전국 대부분 아침 기온 5도 내외…얼음 어는 곳도](https://img.etoday.co.kr/crop/85/60/2098154.jpg)







![[정치대학] 美 대선, 막판까지 초박빙…당선자별 韓 영향은?](https://img.etoday.co.kr/crop/300/170/2098110.jpg)
!['한국의 장 담그기 문화' 유네스코 무형문화유산 등재 유력 [포토]](https://img.etoday.co.kr/crop/300/190/2098066.jpg)